原创 周星星 Ai本草
从2002年6月1日开始施行《中药材生产质量管理规范(试行)》,到2012年、2017年两次修订,再到2022年此次新版中药材GAP的发布,一晃已经20余年。
经历了中药种植、采收、采购混乱无序多年后,内人士才意识到中药材精细化、规范化生产的重要性,也经历了GAP从诞生到推广、修订,再到本次正式发布的一系列进程。在中药材生产供应无法满足民众“绿色、道地、高效”强烈需求的背景下,及时出台符合时代特征的中药材生产质量规范,极为关键。
一、加速推进山西中药材GAP认证,助力中医药高质量发展
随着社会对健康意识的不断提升和对中医药的日益信赖,中医药产业正步入高质量发展的新阶段。消费者对药品质量和安全性的高标准要求,促使整个中医药产业链,特别是中药材的生产管理,必须达到前所未有的严格标准。在此背景下,中药材生产质量管理规范(GAP)的实施显得尤为重要,它涵盖了从土壤、种植、采收到加工等全环节的规范控制,确保了中药材的质量和安全性。
对于中药制药及中药饮片企业来说,标示“药材符合GAP要求”也成为药企实现品牌提档升级和扩大市场份额的重要契机。因为在药品包装上标示“药材符合GAP要求”,等于赋予了药品更高的附加值,使消费者在购买药品时更加放心,也使药品在市场上更具竞争力;甚至还有实实在在的政策红利,如标示后享受集采加分、优质优价(先)等。
山西省拥有丰富的中药材资源和深厚的中医药文化底蕴,被誉为“北药宝库”,但在全国中药材GAP工作推进中,却显得滞后,至今无一药企或品种通过符合性检查(延伸检查),这无疑为山西中药材产业的发展敲响了警钟。
自国家药监局综合司2023年6月12日印发《<中药材生产质量管理规范>监督实施示范建设方案》以来,安徽、甘肃、四川、广东等示范省份积极响应,依据各自区域特色与产业优势,展开中药材GAP监督实施示范建设工作。云南省作为国内首例,创新性地采取了基地评价与延伸检查相结合的方式,取得了显著成效;陕西省则以协会形式参与中药材GAP基地建设,发挥了重要作用;福建省设立了专项资金支持中药材生产基地建设;海南省、天津市和内蒙古自治区则通过省药监局直接与其他省份联合开展相关工作,提高了效率。
截至2024年10月11日,全国已有67家企业、57个品种通过新版中药材GAP符合性检查(延伸检查)。相比之下,山西作为中药材资源大省,其丰富的中药材资源(1788种中药材,39种道地药材)未能得到有效利用和认证,这不仅影响了山西中药材的品牌影响力和市场竞争力,也制约了中医药产业的高质量发展。
在此,呼吁山西省药监局能够主动作为,学习借鉴其他省份的成功经验,创新工作方法,提高工作效率,有序、快速地推进本地中药材GAP的相关工作。
二、对新版GAP的几点建议
首先,应建立不同层次的质量标准
从当前的需求层次分析,中成药、颗粒剂企业关注原料的含量指标;饮片企业、中医临床更关注外观、性价比和实战效果;民众对于药食两用品种则更关注绿色、道地和无公害。
国家在制定中药标准时,应充分考虑这种需求的差异化,建立不同层次的标准体系,而不是一部《药典》吃遍全产业链。两会期间,全国政协常委、国家中医药管理局副局长黄璐琦院士提出《关于制定〈国家中药材质量规范〉的提案》,实际上就是充分考虑了这种需求层次的差异化。
笔者以为理想的路径是:中成药和颗粒剂标准偏重《药典》 ,中药饮片标准偏重于《国家中药材质量规范》,药食两用品种则偏重于蔬菜和粮食无公害标准,这样执行下来的GAP才更“接地气”,更接近市场现实。
其次,应从核心品种实现突破
建议GAP重点突破和关注的品种,一是中医临床不可替代的“帅药”或组方中的“君药”品种,如附子、细辛、半夏、柴胡、人参、大黄等;二是对含量和质量要求较高的品种,如红花、连翘、金银花等,注射剂、颗粒剂原料必须按照GAP标准建立基地并全程质量追溯;三是民众关注度较高、用量较大的品种,如燕窝、三七、党参、当归、黄芪等,但GAP质控的关键点应放在农残、重金属等方面,而不是含量指标。
第三,应从核心环节上实现突破
目前阶段,要想实现全方位的GAP落地不现实,特别是在中药饮片领域,笔者建议先从中医临床最关注的点上实现突破,例如品种来源、用药部位、生长周期、采收时间、加工方式等,分别制定关键控制参数和要求。
明确了上述环节后,在供应流通或中成药、中药饮片集采中划分出不同质量层次。例如黄芪有野生、多年生仿野生种植、3年生和2年生不同层次;细辛有7年根、6年根、5年根;人参有山参、高丽种、大地参和大田参等不同种源、不同种植年份的标识。把具体选择权交给中医临床把握,医生可根据患者病程、病机、消费能力的不同,选择不同质量、不同价位的中药商品;消费者同样可以根据商品标识,自行选择不同质量和价位品种。
第四,应尽可能减轻GAP认证给企业带来的成本负担
一方面,除了政策支持外,国家还应对企业开展GAP基地建设给予一定补贴,甚至GAP免费认证;另一方面,国家应在中成药价格限定、中药集采活动中,允许GAP认证产品价格高于非GAP认证产品;其三,应加大宣传力度,在需求端建立“优质优价”的语境,消化因GAP认证带来的相应成本增长。
最后,应从结果导向来追溯GAP过程
就目前的技术水平和产区分散的现状看,想完全监控GAP全过程几乎是不可能完成的任务,最终只能导致大量数据造假和过程造假。
笔者建议不妨按照GAP的结果来追溯生产过程,例如,不允许使用高毒农药、过量施化肥特别是膨大剂,那么,哪些实验室指标可以验证出这些违法违规行为?从理化指标上,如何导向生长周期、采收时间或加工方式?笔者认为,这才是当前中药检测的核心任务,也是确保GAP标准能顺利实施的“科技利器”。
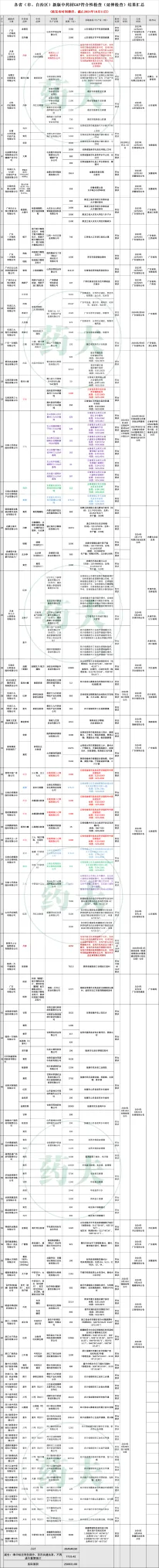
附:全国通过新版中药材GAP符合性检查(延伸检查)的企业、品种名录