本文为个人观点内容的准确、完整与时效性,基于现有公开信息及个人认知水平,受限于信息动态变化与认知局限,可能存在不足。诚邀读者参与校验完善,若发现问题请指正,您的反馈至关重要,有助于提升内容与数据质量。期待携手优化信息服务,共建知识共享生态。
中药材是中医药发展的物质基础,是中药产业和大健康产业的主要原料。因此,确保中药材的质量至关重要。实施《中药材生产质量管理规范》(中药材GAP),有助于推动中药材规范化生产,从源头提升中药质量,促进中药传承创新和高质量发展。此外,中药材GAP有助于对中药材生产全过程进行有效的品质控制,是保证中药材品质“稳定、可控”,保障中医临床用药“安全、有效”的重要措施。 本报告系统梳理国家政策推进路径,对比分析各省(直辖市)政策亮点与实施差异,总结阶段性成果,并提出优化意见。这一整理将有助于理解各地区在实施中药材GAP方面的特色做法和成功经验,仅为个人开展中药材GAP政策宣贯工作提供参考,不足之处敬请指正。 (一)政策发展历程 2002年,国家药品监督管理局发布《中药材生产质量管理规范(试行)》(试行版中药材GAP),并采用认证管理;2003年,配套的认证管理办法和认证检查评定标准相继出台,正式启动认证工作。试行版中药材GAP在提升行业对原料药材质量重视程度、培养专业人才以及推进中药材规范化规模化生产、提高质量方面发挥了积极作用。然而,随着行业的发展,其内容笼统、质量风险管控理念执行不到位、对影响中药材质量的重要环节缺乏明确要求等问题逐渐凸显,导致企业在理解和实施过程中面临诸多困难。2016年3月,依据《国务院关于取消和调整一批行政审批项目等事项的决定》,GAP认证被取消。 为贯彻落实《中共中央国务院关于促进中医药传承创新发展的意见》,推进中药材规范化生产,加强中药材质量控制,促进中药高质量发展,2022年3月,国家药监局、农业农村部、国家林草局、国家中医药局联合发布了《中药材生产质量管理规范》(新版中药材GAP)。新版中药材GAP是中药材生产企业规范化生产的技术指导原则,是中药生产企业供应商质量审核的技术标准以及药品监督管理部门延伸检查的技术依据,为加强中药材生产质量管理提供了新的技术规范,将成为基地企业、中药企业、行业主管部门和地方人民政府发展中药材产业的有力的抓手。 (二)推进实施举措 2023年5月,国家药监局设立中药材GAP专家工作组,旨在发挥行业内技术专家的指导和支撑作用,加快推进新版中药材GAP的有序实施。 2023年6月,国家药监局综合司印发《<中药材生产质量管理规范>监督实施示范建设方案》(简称《方案》),先后两批分别指定安徽、广东、四川、甘肃和河北、山东、江西、云南等8个省级药品监管部门作为任务承担单位,统筹监管与服务,强化协同配合,推动产地引导,促进中药材GAP的稳步实施。随后,国家药监局核查中心发布《中药材GAP实施技术指导原则》和《中药材GAP检查指南》,为实施工作提供技术指导。 2023年8月,国家药监局在兰州召开中药材GAP监督实施示范建设工作推进会,听取了相关省份的进展汇报,并充分肯定了各地的创新措施。 (三)实施效果 截至2025年7月25日,全国共有22个省份(直辖市)公布延伸检查结果,被检查主体和中药材生产企业共计260家,通过中药材GAP符合性延伸检查的中药品种154个。其中,中药饮片64个、配方颗粒25个、注射剂17个、中成药48个。 参考“药夫”公众号统计,现已有121个品种符合新版GAP要求或已通过符合性检查(延伸检查),GAP基地面积共计564424.5亩。这56万余亩的GAP基地与全国约5000万亩的总种植面积相比,仅占1.2%。 据公开信息统计,天津天士力之骄药业有限公司注射用丹参多酚酸成品20231216批开始在包装上增加“药材符合GAP要求”标识。江西省青峰药业有限公司的喜炎平注射液完成标示“药材符合GAP要求”药品标签备案,利君集团现代中药“沙苑子颗粒”则成为陕西省首个在包装上注明“药材符合GAP要求”标识的产品。此外,四川省中药饮片有限责任公司、四川新荷花中药饮片股份有限公司、成都欣福源中药饮片有限公司,可在标签上标示“药材符合GAP要求” (一)共性内容 各地在推动中药材GAP实施过程中,普遍遵循《<中药材生产质量管理规范>监督实施示范建设方案》主要体现在以下几个方面: 遴选重点企业和品种。指导开展自评和报送,制定监督实施示范建设工作实施细则,明确服务企业主动报告的程序和要求。开展延伸检查和公开结果。规范GAP标识管理。成立中药GAP专家组,为实施工作提供技术支持和专业咨询。 (二)差异与亮点 重点企业遴选标准,《方案》明确提出将遴选重点企业和品种列为重点任务。而在各地具体实施过程中,重点企业的遴选标准呈现出差异化特征。 以甘肃为例,龙头企业遴选要求企业需具备显著的社会带动效应。具体要求为,中药生产企业带动农民合作社达到10个以上,签约共建或自有种植基地面积不少于3000亩(不限品种),其中采收面积在1000亩以上。 安徽、广东、四川、河北等省份侧重对企业自身的合规性的考量,强调示范建设单位应有自建、共建、共享符合中药材GAP要求的中药材种植基地,连续三年内无严重违法违规行为,无失信行为信息等要求。 医保部门联动,四川、甘肃、安徽三省作为试点单位,省药监局与医保部门联合发布中药材GAP实施文件。强调使用符合GAP药材的药品纳入带量采购,优先挂网等政策支持,推动“优质优价”、“优质优选”的新秩序。 基地评价与延伸检查相结合,云南省四部门联合印发《云南省中药材 GAP 基地评价管理办法》,在国内首创基地评价与延伸检查相结合的模式,实践中取得显著成效。2024年6月,贵州省农业农村厅发布《贵州省中药材 GAP 基地评价管理办法(征求意见稿)》并公开征求意见,可能会采用基地评价这一创新方式,但相关正式文件尚未出台。 协会参与GAP建设,2023年7月,陕西省药品监督管理局正式批复了《陕西省中药协会关于参与推进陕西省中药材GAP基地建设工作的意见》,同意该协会积极参与陕西省中药材GAP基地建设工作。基地经过验收后颁发《陕西省GAP药源基地认定证书》,认定期限为一年。陕西作为国内首例以社会团体(协会)形式参与中药材 GAP 基地建设的实践,为行业探索了新路径。 资金激励政策方面,多个省份已出台明确举措。其中,福建省通过《福建省贯彻落实<中药材生产质量管理规范>实施意见》设立专项资,对建设道地药材100亩以上规范化全过程可追溯种植基地,产品符合国家或省级标准的,经评审合格给予每个种植基地50万元奖励,每个单位每年支持额度不超过100万元。 云南则在《云南省中药材GAP基地评价奖补资金申报指南》中明确指出,2025—2027年,按照“先建后补、先评后补”的原则,对省内通过中药材GAP基地评价,且基地种植面积100亩以上或养殖面积10亩以上的经营主体,给予一次性50万元奖补。 湖北省在《湖北省推进中药材生产质量管理规范实施意见》提出,各级各部门要制定推进实施中药材GAP的激励政策,统筹用好项目资金、税收优惠、农业保险、土地流转等各项扶持政策。此外,全国其他省份也结合本地产业特点,围绕绕中药材规范化种植、中药材产地规范化加工、药用动物规范化养殖、全程可追溯体系、林下经济等方向推出多样化激励政策。 指导性参考文件,重庆印发《重庆市中药材生产质量管理规范延伸检查技术参考,通过对照中药材GAP核心内容逐条解析检查要点,为企业科学实施中药材GAP提供精准指引。山东省发布《山东省中药材生产质量管理规范建设指导手册》,从生产基地建设规划、文件撰写、生产基地建设、生产管理与质量控制、内审完善和中药材生产追溯体系六部分内容,以“手把手”指导企业构建符合中药材GAP质量管理体系,确保种养殖全流程可追溯,真正达到中药材GAP要求。此外,云南省药监局印发的《云南省中药材GAP检查细则》,则明确了检查对象、总体要求、13个检查板块具体内容、检查流程及资料审查要求等,对统一全省中药材GAP检查尺度、推动云南省中药材GAP落地实施、从源头保障中药材质量安全有效、促进云南省中药产业高质量发展具有重要意义。 延伸检查和结果公开,从各省延伸检查公示信息来看,绝大多数省份均公开了被检查主体(药品生产企业)、被检查品种(药品名称)、中药材品种、中药材企业、基地地址、基地面积、坐标信息等项目。其中,内蒙古、上海、安徽、福建、辽宁、陕西、甘肃、海南等省份在还根据地方管理特点或实际检查情况,补充公开了年产量、建设模式、检查时间、批号、共建单位、种植面积、认定时间、截止时间等特色信息。 总体而言,尽管各省在信息公开和特色补充内容上存在一定差异,但这些差异并未对中药材GAP工作的整体推进和监管效能构成实质影响。 《方案》要求,结合本辖区中药发展和中药材生产的实际,遴选重点中药生产企业使用5—10种符合GAP的中药材生产重点品种。遴选过程中应当聚焦规范化发展基础较好的中药材品种,结合重点中药生产企业进展,按照中药监管相关规定和要求优先选择中药注射剂,中药配方颗粒,采购产地加工(趁鲜切制)中药材生产的中药饮片或者其他中成药大品种作为重点品种等。 截至2025年7月25日,全国34个省级行政区中已有22个省(自治区、直辖市)公示了中药材GAP延伸检查结果。8个试点省份中,以甘肃被检查主体数量最多,但未公示中药品种。其次为云南,以基地评价和延伸检查相结合的创新形式公示18家被检查主体。详细情况如下表。 数据管理混乱:中药材生产企业和农户在数据记录环节普遍存在严重缺陷,信息缺失、错误频出。这使得生产过程中的关键数据无法有效支撑科学管理决策,如施肥量、农药使用和喷洒量、病虫害发生时间与程度等数据的不准确,导致无法精准调控生产,影响中药材质量稳定性,也给后续质量追溯和问题排查带来极大阻碍。 农户技术匮乏:广大农户作为中药材种植的一线生产者,在GAP相关技术知识和操作技能方面极度欠缺。在科学选种、合理施肥、精准病虫害防治以及规范采收等核心环节,缺乏必要的专业指导和培训,严重依赖传统经验,难以适应现代化、规范化的GAP生产要求,成为制约中药材品质提升的关键瓶颈。这就容易导致企业溯源和文件体系脱钩,变成“为了追溯而追溯”。 执行尺度差异显著:不同地区和企业对GAP标准的理解与执行尺度不一,缺乏统一权威且细化的延伸检查方案和实施准则,导致企业实际操作中无所适从,不知从何入手,同时阻碍了各省协同互认结果。 跨省互认机制落实不足,尽管《方案》明确鼓励省级药品监管部门在沟通基础上互认已完成的延伸检查结果,但实际执行中互认程度较低。根据公开信息显示,在自建、共建、共享方式建GAP基地模式中,部分企业面临重复检查:例如,有中药材生产企业已被3个省份延伸检查,也有中药材产企业被2个省份检查,甚至个别企业在本省内亦被多次检查。这不仅增加企业负担,也反映了互认机制未能有效落地。 为进一步推进实施中药材GAP,规范中药材种植、加工、销售全流程管理,需构建标准化、常态化的监管与能力提升体系,具体可从四方面推进: 一是制定统一实操手册,由主管部门牵头,联合行业权威机构、行业协会等,共同编制全面细致的实操手册,囊括生产基地建设规划、文件撰写、生产基地建设、生产管理与质量控制、内审和中药材生产追溯体系等内容,并将标准操作规程制定模板、质量标准制定模板、管理制度制定模板及示例作为附件,“手把手”指导中药材生产企业建设中药材GAP基地。 二是统一延伸检查方案,基于实操手册建立全国统一的延伸检查,涵盖生产各环节的核心质量控制点、合规性要求等,确保各地监管尺度一致,避免因标准差异导致的监管失衡。 三是建立结果互认与持续监管机制,推动各地检查结果跨区域互认,减少重复检查对企业的负担;同时,变“一次性认证”为持续性、不定期检查机制,通过动态监管强化企业主体责任,确保中药材GAP长效落实。 四是系统提升企业专业水平,定期组织系统性、针对性强的GAP技术培训活动,邀请行业专家结合丰富的实践案例进行具有实操性的讲解,帮助企业精准把握规范要点;同步搭建便捷高效的在线学习平台,整合视频教程、互动答疑、模拟实践等多维度,满足企业碎片化学习需求与个性化提升方向,助力其持续更新专业技能、夯实知识储备,从主体能力层面筑牢中药材质量保障基础。一、前言
二、政策出台与实施情况
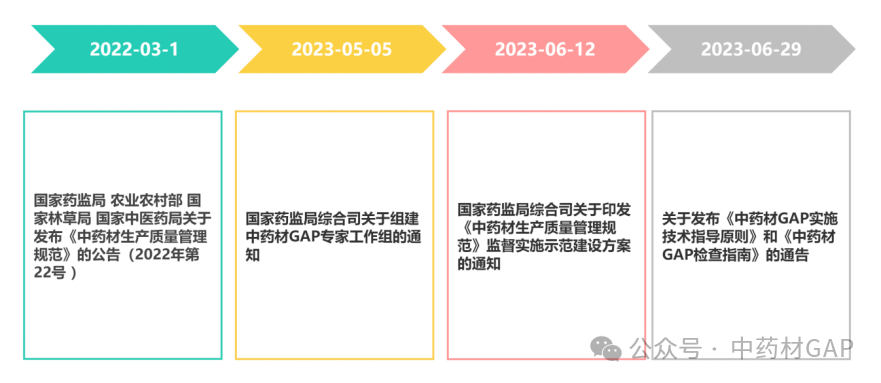

三、各地政策实施亮点和不同
四、各地实施进展
(一)各省分实施进展
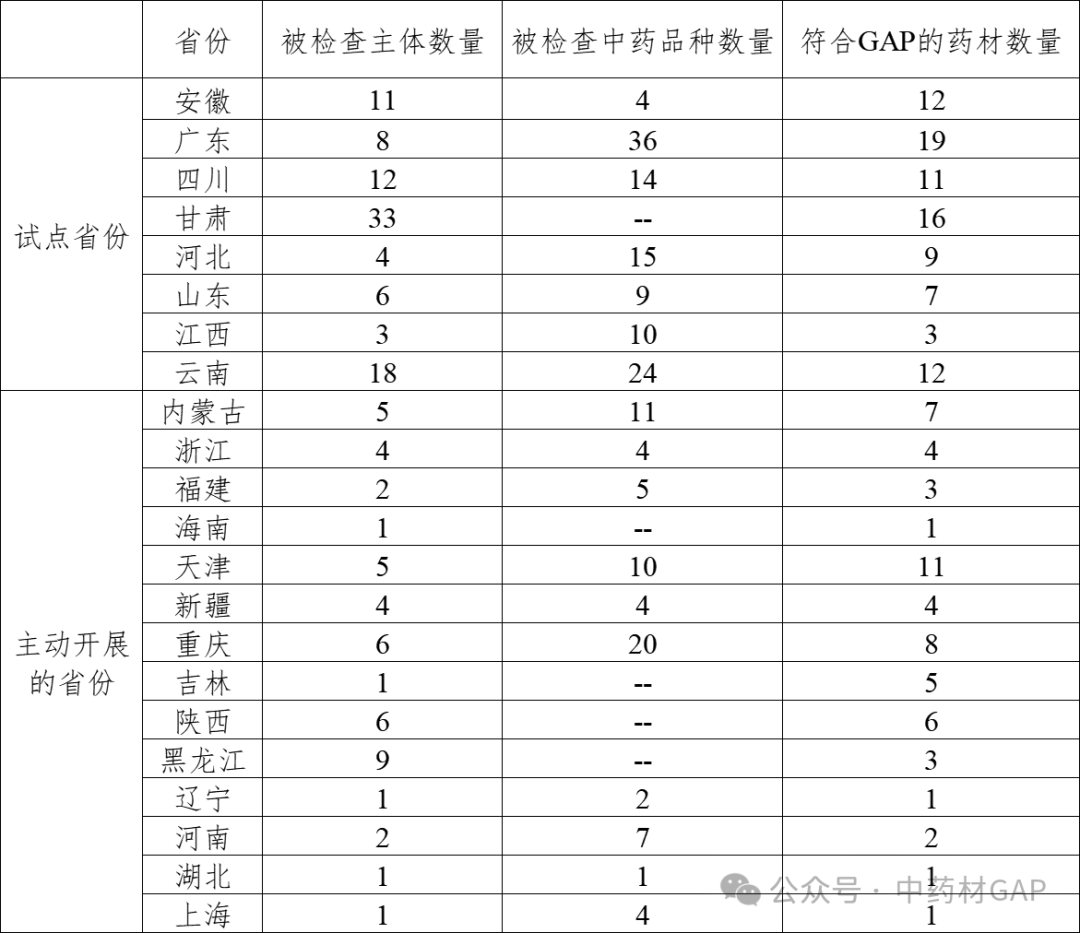
四、存在的问题和建议
(一)存在的问题
(一)实施建议




